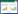文章信息
- 周兆熊, 袁键键, 邵华, 殷万武, 王成勇
- ZHOU Zhaoxiong, YUAN Jianjian, SHAO Hua, YIN Wanwu, WANG Chengyong
- 血管介入治疗导丝推进力与血管阻塞体强度及长度特征关系试验研究
- Experimental study on the relationship between the force of guide wire in mechanically assisted vascular intervention and the strength and length of vascular obstruction
- 中国测试, 2019, 45(7): 31-36
- CHINA MEASUREMENT & TEST, 2019, 45(7): 31-36
- http://dx.doi.org/10.11857/j.issn.1674-5124.2017070044
2. 上海交通大学机械与动力工程学院,上海 200240;
3. 广东工业大学机电工程学院,广东 广州 510006
2. School of Mechanical Engineering, Shanghai Jiao Tong University, Shanghai 200240, China;
3. School of Electromechanical Engineering, Guangdong University of Technology, Guangzhou 510006, China
微创外科手术[1]的出现为医学领域翻开新的篇章。血管介入治疗是微创外科的一个新方向,其具有出血少、创伤小、并发症少、安全可靠、术后恢复快等优点[2]。传统血管介入治疗手术是通过医师的手指触觉来感知,缺乏精确的力的反馈,其操作精度低。精确的力反馈信号能支撑医生对组织状况做出准确判断,从而提高手术的成功率。
近年来,国内外在导丝输送力信号方面的研究主要有:南京航空航天大学的冯安祥[3]采用球包围盒的碰撞算法,建立了力反馈计算模型,具有一定的实时性和精度。上海交通大学的盛国栋[4]基于3DS MAX的建模及力触觉渲染引擎CHAI 3D进行仿真,来模拟脊柱手术平台。上海交通大学的王丽娟[5]采用基于PI参数自整定与阻抗控制相结合的控制策略对系统进行力反馈控制。Lenoir[6]等建立血管模型,通过有限元法对模型的力信号进行了精确的计算。然而以上研究并没有对算法及系统进行验证,仅在理论上证明可行。
哈尔滨工业大学的付宜利[7]教授认为力反馈主要有直接反馈和感知替代两种方法。Christopher J. Payne等[8]通过研究表明力反馈系统减少了模拟血管内手术期间施加的力的大小和持续时间。然而其并不能提供精确的力信号,从而不能判断阻塞体的阻塞程度。另外一些研究人员通过将传感器贴于导丝头来实时感知力信号[9-10],该方法对人体的排异反应缺乏考虑,增加临床的危险性。
目前血管阻塞诊断的方法包括动脉造影技术、超声诊断及磁共振等。传统的血管造影技术已在临床运用了几十年[11],冠状动脉造影术(CAG)是诊断冠心病的“金标准”[12],可以清楚显示心脏冠状动脉粥样硬化造成的血管内腔不规则狭窄,并且可做介入治疗,如球囊扩张或放置血管内支架。然而造影技术属于创伤性检查,且并发症较高(6%)。超声具有简便、无创、可重复、准确快速等特点[13],但超声检查受人体血管纵横交错的复杂性限制,不能提供明确的定位。磁共振血管造影(MRA)可清晰地显示椎动脉狭窄和阻塞的位置[14],但也必须注射造影剂才能增强扫描,且适合大血栓,不具有广泛性。
为实现实时精确的力反馈,本文结合现有技术的优缺点,基于全桥应变梁搭建了导丝位置实时反馈及力信号采集的机械辅助血管介入治疗装置。在该装置基础上,对血管介入治疗导丝运动过程进行分析并展开阻塞血管中导丝推进力监测试验。
1 机械辅助血管介入治疗过程中导丝运动过程分析血管阻塞及畸形治疗过程中,为实现对血管的扩张、支架的安放和溶栓药剂的释放,需利用导丝穿透阻塞物质。血管阻塞的原因多为血液内粘性物质如脂肪、胆固醇和血小板等发生堆积。该类物质具有一定强度,需要一定大小的力进行穿刺。
直头导丝匀速穿刺血管阻塞物的过程,如图1所示。随着输送的进行,导丝前端与阻塞体表面产生接触。由于阻塞体具有一定强度,导丝无法立即刺入对阻塞体。导丝的继续输送引发导丝轴向弯曲变形。导丝弹性势能逐渐增加,与阻塞体表面的接触力也逐渐增大。当接触位置的压强高于阻塞体强度,导丝刺穿阻塞体,自身的弹性势能释放,输送阻力下降。随着进入阻塞体的导丝长度不断增加,两者的接触面积逐渐增大,输送阻力迅速增加。软粘的阻塞体对导丝输送的阻滞作用远高于血液,阻塞体中导丝输送阻力时域信号斜率较无阻塞血管内输送阻力信号的斜率大。
|
| 图 1 直头导丝匀速穿刺过程 |
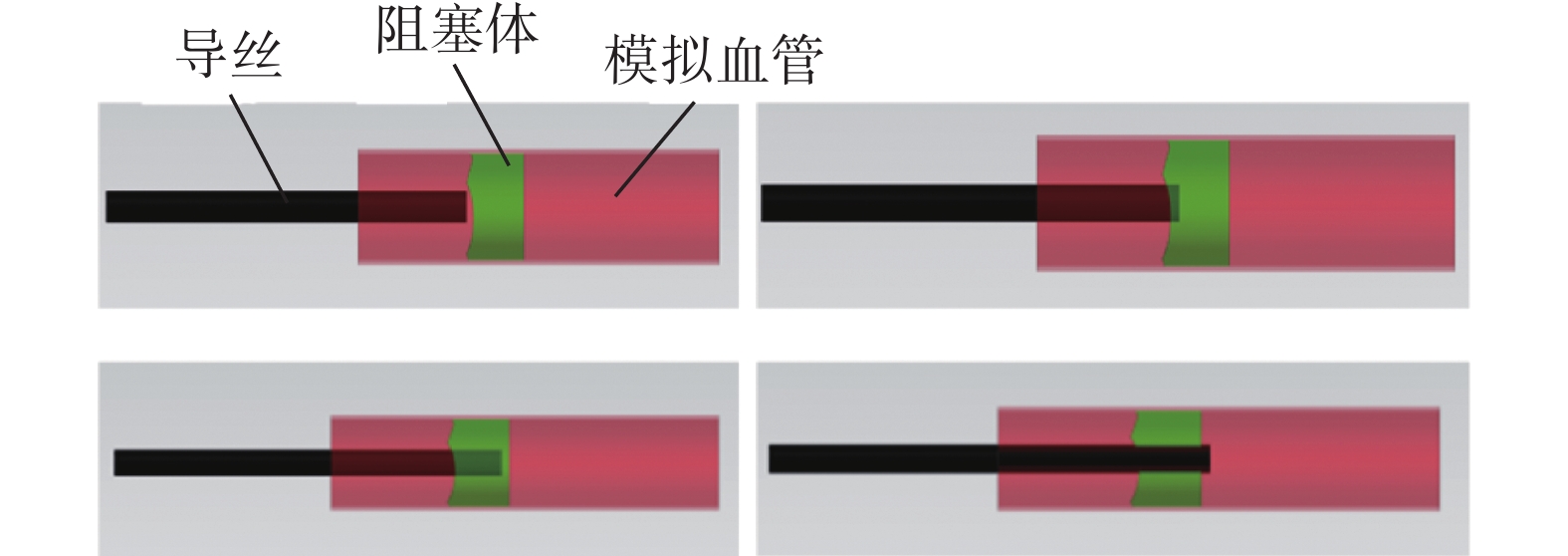
如图2所示,分析导丝输送过程中阻力变化情况可以发现,在导丝刺入与刺出阻塞体时刻输送阻力出现信号尖峰。当输送速度已知,基于导丝刺入与刺出阻塞体的时刻,可获得导丝在阻塞体内的输送距离。当血管直径较小,阻塞体内导丝在血管径向的弯曲变形可忽略不计。此时,导丝在阻塞体内的输送距离与阻塞体长度相等。阻塞体长度可如下计算:
|
| 图 2 导丝输送阻力与输送长度关系 |
| ${{{L}}_{{\rm{zu}}}} = {{v}} \times \left( {{{{t}}_{{\rm{end}}}} - {{{t}}_{{\rm{begin}}}}} \right)$ | (1) |
式中:Lzu——阻塞体长度,mm;
v——导丝匀速输送速度,mm/s;
tend——导丝刺出时刻,s;
tbegin——导丝头部接触阻塞体表面时刻,s。
导丝刺破阻塞体的穿刺力由两者的接触面积与阻塞体强度决定,可表示如下:
| ${{{F}}_{{\rm{ci}}}} = {{S}} \times {{{P}}_{{\rm{zu}}}}$ | (2) |
式中:Fci——导丝刺穿阻塞体的力,N;
S——导丝与阻塞体接触面积,mm2;
Pzu——阻塞体强度,MPa。
清晰地识别出血管阻塞的强度及长度是治疗心血管疾病的前提及依据。基于机械辅助血管介入治疗中血管阻塞体长度及强度问题,提出将导丝直接作用于阻塞血管并实时测量的方法。搭建导丝输送及测量的装置,并进行试验验证。
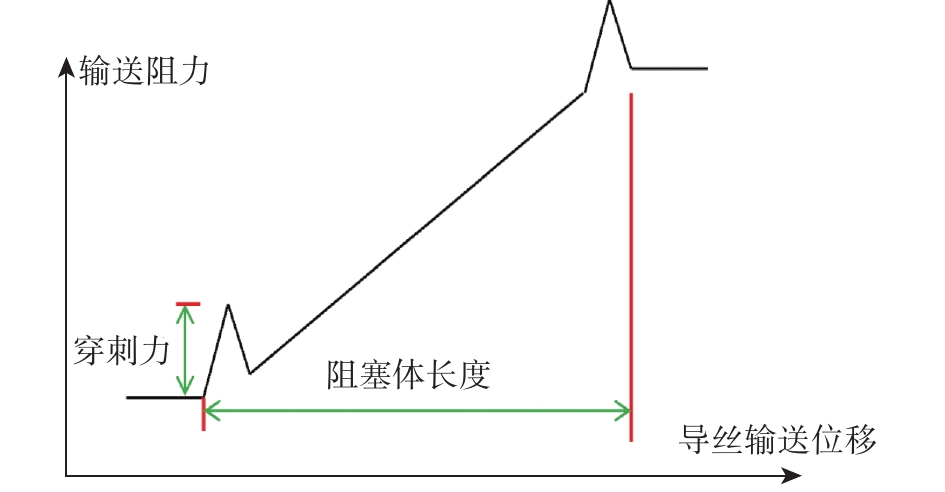
2 试验装置和方法 2.1 试验装置导丝输送力测量系统由夹具、应变梁、安装基座3个部件组成。应变梁一端与夹具通过螺栓连接,一端与安装基座连接。装置简图如图3所示。在输送过程中,导丝由夹具带动匀速进行轴向穿刺阻塞体运动。该导丝输送力的反作用力直接作用于应变梁,使其产生变形。应变梁上下表面贴有应变片,组成全桥电路,在该变形作用下输出模拟电压量。信号放大后,经数据采集卡获得电压序列信号。
|
| 图 3 导丝输送力测量装置简图 |
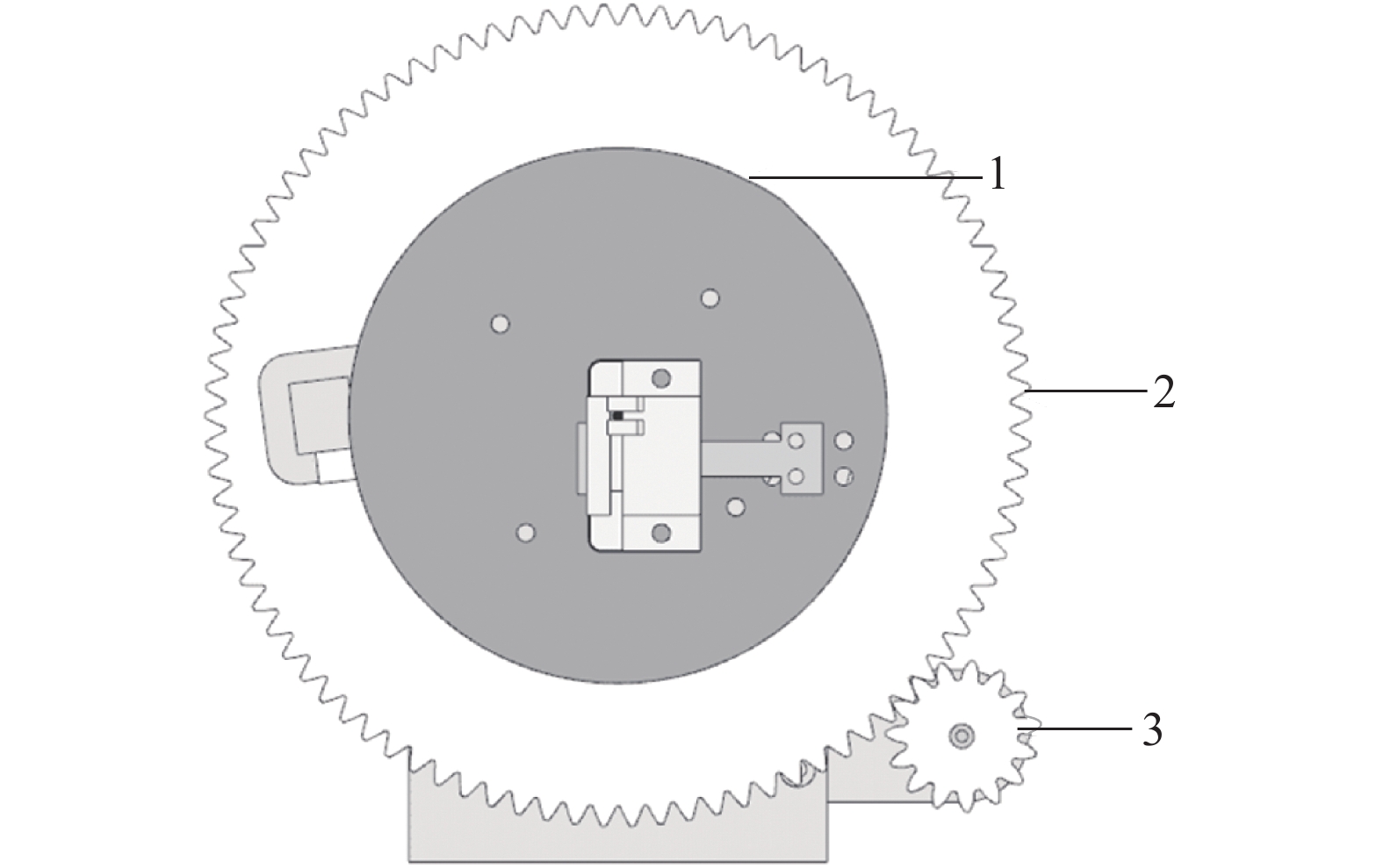
导丝的输送运动由轴向匀速平移运动和以轴线为旋转中心的转动组成。导丝输送力测量装置安装于从动轮,在电机的带动下实现导丝以轴线为中心的转动。装置安装方式如图4所示。在搭建导丝输送及力信号测量装置基础上,为探究阻塞体形态变化对导丝输送过程中的特征力影响,需对导丝在穿刺阻塞血管时力信号变化进行定性分析。
|
| 图 4 导丝输送力测量装置安装简图 1.导丝输送力测量装置;2.从动轮;3.主动轮。 |
2.2 试验原理及方法
输送阻力测量系统的原理是输送过程中导丝在夹具施加的输送力下进行沿血管轴向的匀速直线输送运动,该输送力等于导丝输送阻力。导丝对应变元件的反作用力使得应变梁产生变形。应变梁上下表面贴有应变片,并组成全桥电路。在变形的作用下,全桥电路输出表征变形程度的电压信号。输出的模拟电压信号为毫伏级,为降低信号干扰产生的误差,采用差分放大电路对其进行增益。放大后的电压信号被数据采集卡采集转化为电压序列,经LabVIEW编程实时显示力信号图。输送阻力测量系统电路原理如图5所示。

|
| 图 5 输送阻力测量系统电路原理图 |
为分析阻塞体强度对直头导丝输送阻力的影响,从穿刺力和阻塞体内运动段输送阻力斜率的角度进行阻塞血管输送状态下直头导丝输送试验。
试验条件:
1)检测设备:导丝输送阻力测量系统;
2)被测对象:直头导丝在不同强度阻塞体中的输送阻力;
3)试验方式:测量不同阻塞体强度的阻塞血管输送状态下直头导丝的输送阻力。
试验中采用明胶水溶液的凝胶作为血管阻塞体的模拟。通过改变溶液浓度控制阻塞体强度实现对不同类型阻塞体的模拟。为分析阻塞体强度及长度对直头导丝输送阻力的影响,从穿刺力和阻塞体内运动段输送阻力斜率的角度进行阻塞血管输送状态下直头导丝输送试验。
实验方法:针对阻塞体的软粘特性,试验中选用明胶水溶液的凝胶模拟阻塞体,控制明胶水溶液浓度实现对阻塞体强度的控制。选用的明胶水溶液质量浓度为3%、6%、9%,模拟血管长度有19,30 ,37,38 mm。试验在相同血管直径的模拟血管中进行,选择的血管直径为4 mm。图6为实验示意图。

|
| 图 6 阻塞血管中直头导丝匀速输送示意图 |
3 试验结果及分析
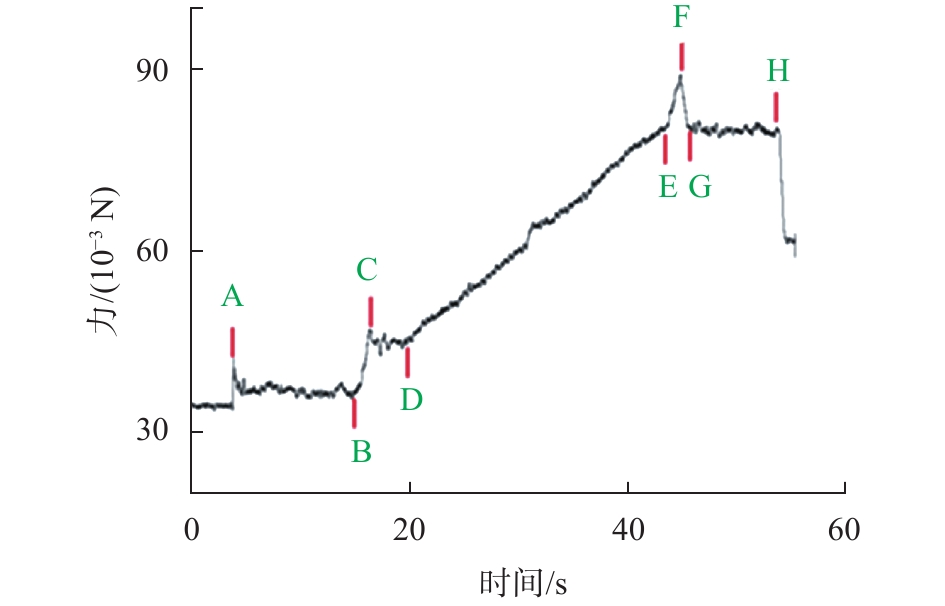
阻塞血管输送状态下直头导丝的输送阻力时域信号呈现带有尖峰的倾斜直线。图7为直头导丝在血管直径为4 mm,模拟阻塞体的明胶凝胶质量浓度为6%条件下的输送信号。
|
| 图 7 阻塞血管中直头导丝输送阻力结果 |
图中节点A为输送开始时刻。节点A-B段为导丝在直线血管中输送,其信号特征为平缓直线。节点B为导丝前端与阻塞体接触时刻,此时接触力较小,无法刺破阻塞体。随着输送的进行,导丝逐渐产生弯曲变形,输送阻力不断增大。节点C为导丝刺穿阻塞体的时刻。导丝刺破阻塞体后,存储的弹性势能释放,变形减小,输送阻力降低。随着导丝不断进入阻塞体,导丝承受的摩擦阻力不断上升,呈近似线性增长。节点E时刻导丝前端接触阻塞体右侧表面,即将穿透阻塞体。节点F为导丝穿透阻塞体时刻。刺破阻塞体后,导丝继续匀速输送。此时,导丝在阻塞体内的接触状态保持稳定,导丝的输送阻力恒定。节点H时刻输送停止。
试验中,记录导丝刺穿阻塞体表面前的输送阻力与刺破时刻的输送阻力,两者的差值即为直头导丝刺穿阻塞体的穿刺力。提取导丝在阻塞体内运动时段内输送阻力的斜率表征阻塞体对导丝输送的阻滞作用。
试验中采用的参数和提取的穿刺力如表1所示,随着凝胶质量浓度增加,穿刺前阻力、刺穿力和输送阻力斜率均增大,表明阻塞体越难穿刺。
| 试验
编号 |
浓度/
% |
刺穿前阻力/
(10−3 N) |
刺穿时刻阻力/
(10−3 N) |
穿刺力/
(10−3 N) |
输送阻力斜率/
(10−3 N∙s−1) |
| 1 | 3 | 25.71 | 26.76 | 1.058 | 0.255 |
| 2 | 3 | 26.49 | 27.52 | 1.029 | 0.314 |
| 3 | 6 | 36.67 | 45.76 | 9.085 | 1.499 |
| 4 | 6 | 35.88 | 46.76 | 10.88 | 1.303 |
| 5 | 9 | 54.19 | 73.40 | 19.21 | 2.871 |
| 6 | 9 | 31.49 | 49.95 | 18.46 | 2.950 |
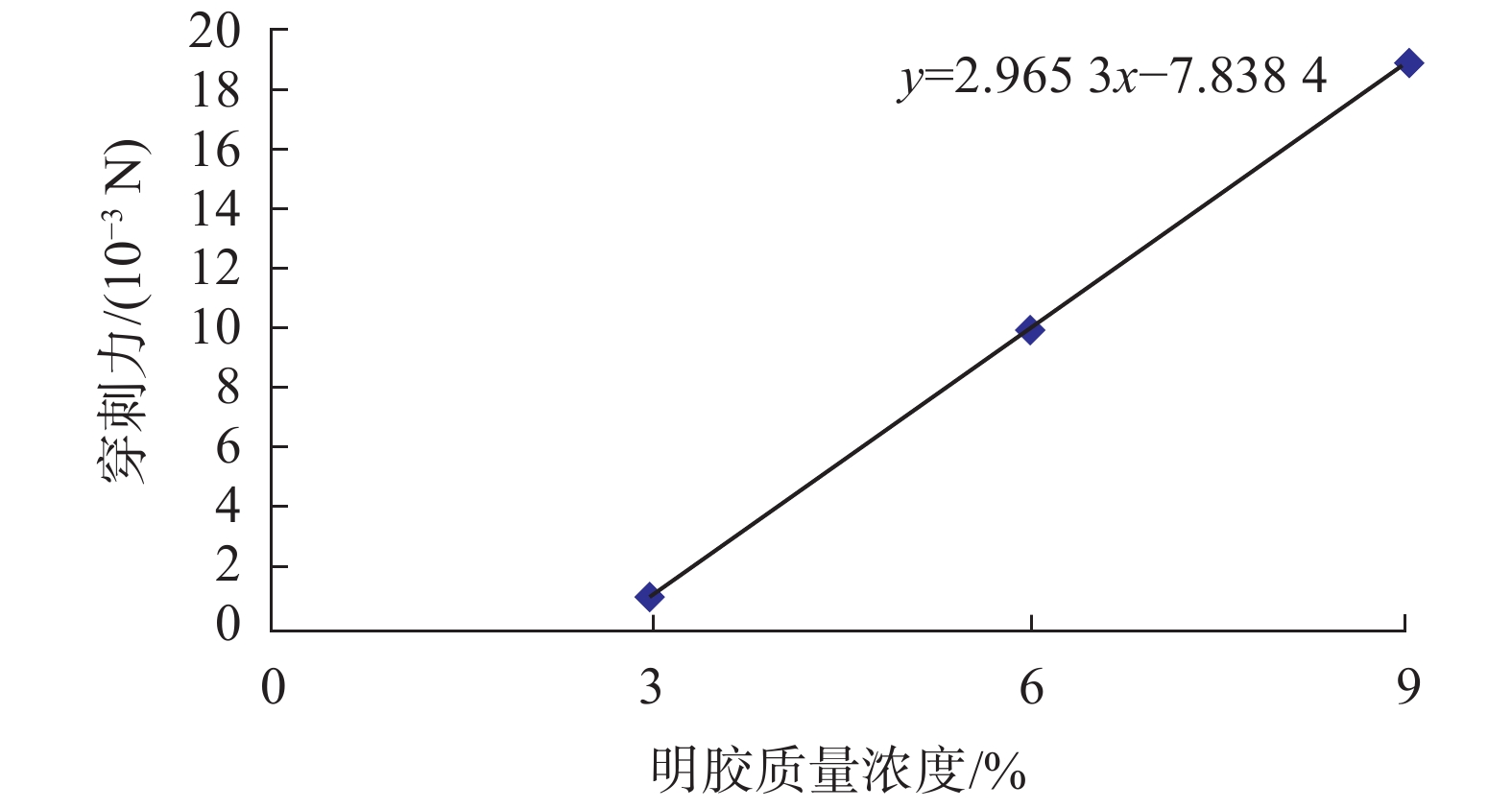
对相同浓度条件下的穿刺力取平均,绘制穿刺力与明胶质量浓度的关系曲线,如图8所示。
|
| 图 8 穿刺力与明胶质量浓度关系 |
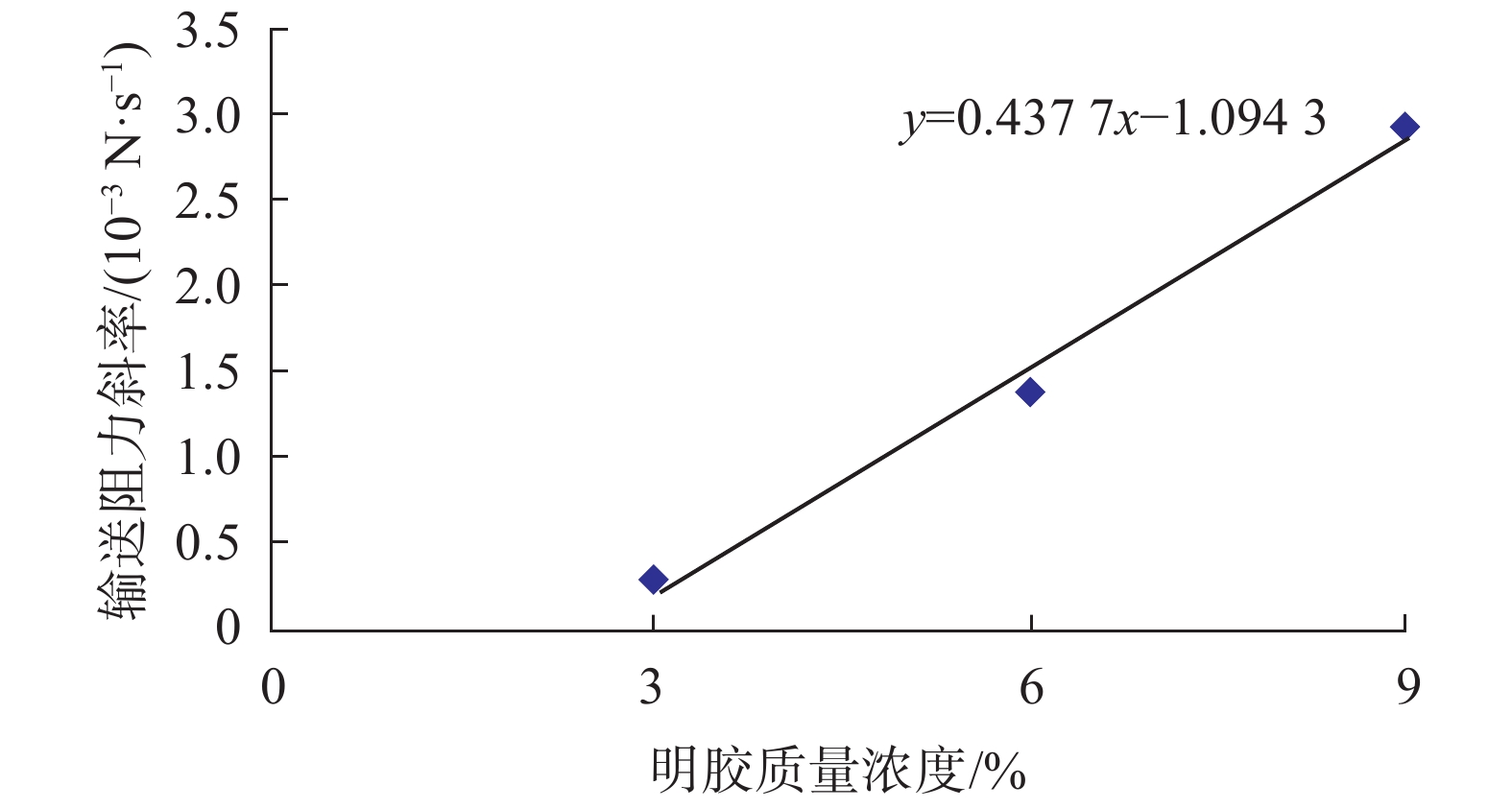
对相同浓度条件下的输送阻力斜率取平均,绘制输送阻力斜率与明胶质量浓度的关系曲线,如图9所示。
|
| 图 9 输送阻力与明胶质量浓度关系 |
由图8分析知:导丝穿刺力与明胶溶液质量浓度呈高度线性相关。随着溶液浓度的提高,穿刺力增大,输送阻力时域信号中表征穿刺过程的尖峰明显程度越高。造成该现象的原因是在同型号导丝与阻塞体的接触面积相同,穿刺力与凝胶强度成正比关系。试验中选用的溶液质量浓度与凝胶强度成正比关系。因此试验中穿刺力与明胶溶液质量浓度成正比关系。
由图9分析知:输送阻力斜率与明胶溶液浓度呈线性相关。随着溶液浓度的提高,输送阻力斜率逐渐增大。造成该现象的原因是溶液浓度越高,阻塞体强度越大,对导丝输送运动的阻滞作用越明显。
当输送速度已知,基于导丝刺入与刺出阻塞体的时刻,可获得导丝在阻塞体内的输送距离。当血管直径较小,阻塞体内导丝在血管径向的弯曲变形可忽略不计。此时,导丝在阻塞体内的输送距离与阻塞体长度相等。阻塞体长度可由公式(1)计算。
依据该信号特征,记录导丝刺入与刺出时刻数据,结合输送速度,推算阻塞体长度。阻塞体的实际长度由直尺测量并记录,如表2所示。分析阻塞体实测与推算长度对比情况可知:基于输送阻力刺入、刺出尖峰信号推算的阻塞体长度与阻塞体实际长度基本一致,相对误差低于5%。
| 试验
编号 |
实测长度/
mm |
刺入时刻/
s |
刺出时刻/
s |
推算长度/
mm |
相对误差/
% |
| 1 | 38 | 20.82 | 59.8 | 39.00 | 2.636 |
| 2 | 38 | 20.08 | 59.1 | 39.02 | 2.663 |
| 3 | 30 | 15.27 | 45.8 | 30.54 | 1.803 |
| 4 | 19 | 17.31 | 36.9 | 19.60 | 3.168 |
| 5 | 37 | 19.18 | 57.3 | 38.10 | 2.986 |
| 6 | 38 | 28.99 | 66.0 | 37.05 | −2.510 |
4 结束语
本文针对微创手术阻塞体穿刺过程展开研究,搭建了阻塞体穿刺阻力测量装置,并通过实时测量实验得到阻塞血管中直头导丝在匀速输送状态下的输送阻力呈现带有尖峰的倾斜直线。信号尖峰出现在刺入与刺出阻塞体时刻,该峰值为刺穿阻塞体的穿刺力。在导丝型号相同的条件下,穿刺力和阻塞体内导丝输送阻力斜率与阻塞体强度成线性正相关。刺入刺出时刻信号尖峰可用于阻塞体长度的预测。试验表明基于信号尖峰推算与实测的阻塞体长度相对误差低于5%。临床中,阻塞体长度的准确获知,有助于医生选用最佳尺寸的球囊导管,支架等治疗器械,降低因器械选择失误造成的时间和资金损失。
| [1] |
TAYLOR R H, STOIANOVICI D. Medical robotics in computer-integrated surgery[J].
IEEE /Transactions on Robotics and Automation, 2003, 19(5): 765-781.
DOI:10.1109/TRA.2003.817058 |
| [2] |
HANSEN MEDICAL. Sensei X Robotic system[EB/OL]. [2011-05-29]. http://www.hansenmedical.com/us/en/vascular/magellan-robotic-system/product-overview.
|
| [3] |
冯安祥, 陈笋, 陈柏, 等. 血管介入手术手术中的柔性虚拟力触觉系统研究[J].
南京信息工程大学学报, 2014, 6(6): 520-524.
DOI:10.3969/j.issn.1674-7070.2014.06.005 |
| [4] |
盛国栋, 曹其新. 基于力反馈的虚拟脊柱手术的模拟系统构建[J].
电子应用技术, 2013, 39(12): 129-131.
|
| [5] |
王莉娟. 虚拟手术力反馈人机交互控制系统研究[D]. 上海: 上海交通大学, 2010
|
| [6] |
LENOIR J, COTIN S, DURIZE C, et al. Interactive physically-based simulation of catheter and guidewire[J].
Computer & Graphics, 2006, 30(3): 416-422.
|
| [7] |
付宜利, 李坤, 潘博, 等. 微创手术机器人力检测与力反馈技术研究现状[J].
机器人, 2014, 36(1): 117-128.
|
| [8] |
PAYNE C J, RAFII-TARI H, YANG G Z. A force feedback system for endovascular catheterisation[C]//2012 IEEE/RSJ International Conference on Intelligent Robots and Systems. IEEE, 2012: 1298-1304.
|
| [9] |
赵德朋, 刘达. 血管介入手术机器人系统力反馈的模糊融合[J].
机器人, 2013(1): 60-66.
|
| [10] |
王焕然. 微创手术导管侧壁触觉传感器的研究[D]. 哈尔滨: 哈尔滨工程大学, 2008.
|
| [11] |
景在平, 赵珺. 影像学技术在血管外科的应用[J].
中国医学影像技术, 2000, 18(9): 857.
|
| [12] |
刘道志. 微创介入医疗器械与材料产业现状和发展趋势[J].
上海生物医学工程, 2007, 28(1): 36-39.
DOI:10.3969/j.issn.1674-1242.2007.01.009 |
| [13] |
刘舜辉, 刘倚河, 郑玉凤, 等. 彩色多普勒超声对周围血管阻塞性疾病的诊断分析[J].
中国全科医学, 2008, 11(8): 702-703.
DOI:10.3969/j.issn.1007-9572.2008.08.027 |
| [14] |
谷奕诺, 张浩. 椎动脉狭窄及阻塞的磁共振血管造影相关影像学研究[J].
中国心血管病研究, 2016, 14(7): 646-650.
DOI:10.3969/j.issn.1672-5301.2016.07.019 |
 2019, Vol. 45
2019, Vol. 45